南科大龚欣团队揭示哺乳动物鞘脂合成的关键负反馈调控机制
日期:2023-07-14
近日,南科大生命科学学院龚欣团队最新的研究成果以“Ceramide sensing by human SPT-ORMDL complex for establishing sphingolipid homeostasis”为题发表在Nature Communications杂志上,揭示了人源SPT-ORMDL复合物通过感应鞘脂合成中间产物神经酰胺的水平,从而负反馈调控鞘脂合成的关键机制。
鞘脂(Sphingolipids)是哺乳动物细胞中的重要膜成分和生物活性分子,参与了多种重要的生命活动。生物体内鞘脂水平需要维持在一个平衡的状态,稳态失调可能导致多种疾病的发生,如肌萎缩侧索硬化症(ALS)、心血管疾病和神经退行性疾病等。哺乳动物鞘脂从头合成的第一步,是由内质网膜上的SPT复合物所催化的,ORMDLs蛋白是SPT的关键负调控蛋白,可以和SPT形成稳定的复合物并直接调控SPT的活性,从而调控细胞内鞘脂的稳态。在哺乳动物细胞中ORMDLs存在三种亚型ORMDL1/2/3,人源ORMDL3基因与儿童哮喘的易感性密切相关。SPT-ORMDL复合物在哺乳动物中的鞘脂生物合成、稳态调控以及多种病理生理过程中都起着至关重要的作用。为了阐明SPT-ORMDL复合物在哺乳动物中发挥作用的机制,龚欣课题组针对人源SPT-ORMDL复合物展开研究。
研究团队首先通过优化体外重组表达、纯化的方法获得了人源SPT-ORMDL复合物的蛋白,并且通过体外酶活实验发现SPT-ORMDL的活性可以被鞘脂生物合成途径中的重要中间产物神经酰胺抑制。为了研究神经酰胺调控SPT-ORMDL活性的结构基础,研究人员利用单颗粒冷冻电镜技术解析了人源SPT-ORMDL3复合物与神经酰胺结合的高分辨率三维结构(图1)。通过后续的生化实验,研究人员发现神经酰胺的结合对SPT活性的抑制具有重要作用,也证明了神经酰胺结合可以诱导并稳定ORMDL3的N端插入到底物结合位点,从而抑制SPT的活性。最后,研究人员还通过体外实验,证明了近几年报道的青少年ALS相关的SPT亚基突变,会导致SPT-ORMDL3突变体蛋白不能被神经酰胺有效抑制。

图1. 人源SPT-ORMDL3复合物与神经酰胺结合的整体结构
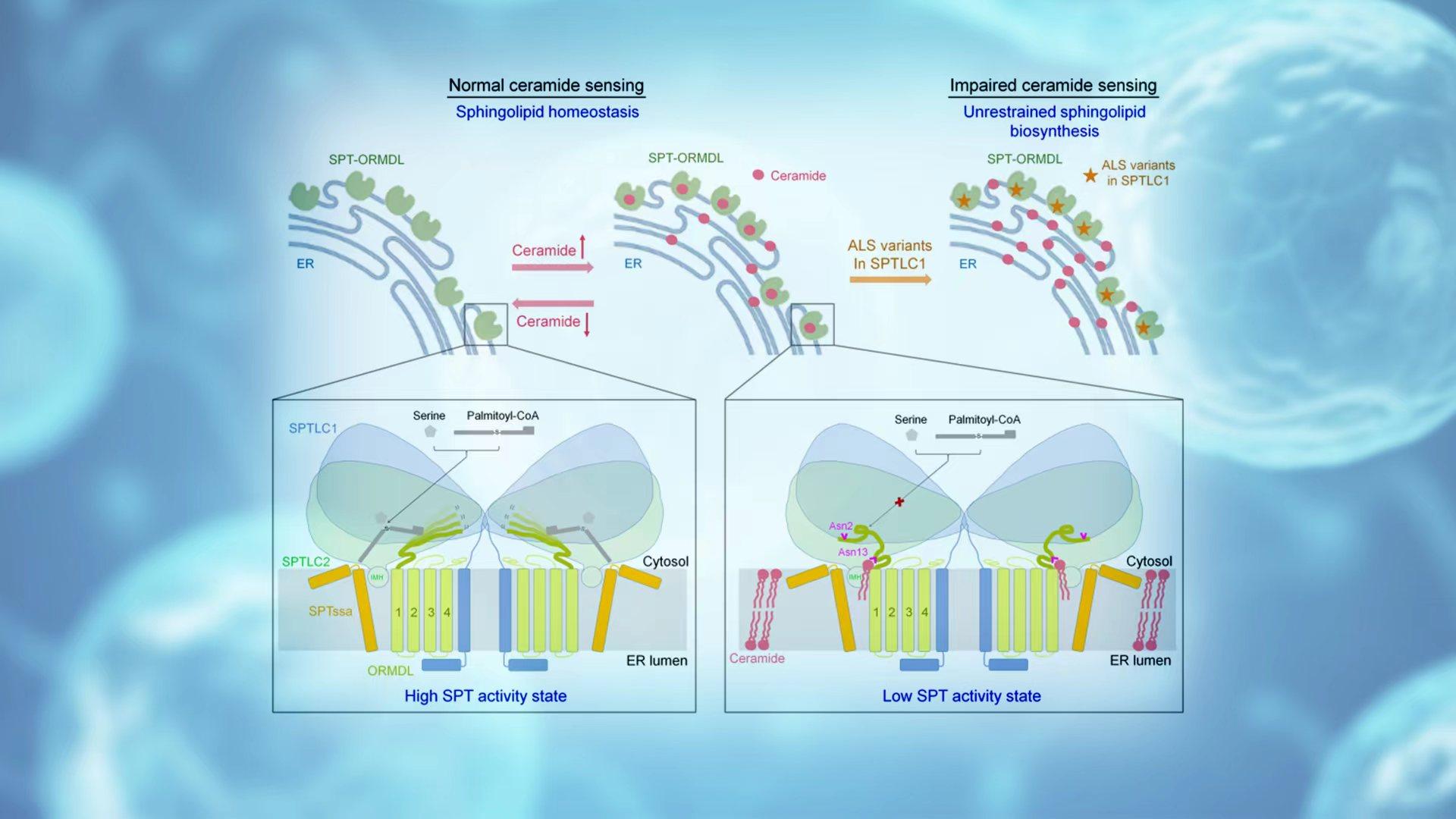
基于本研究中的结构和生化实验结果,研究人员最后提出了一个神经酰胺参与SPT-ORMDL复合物稳态调控的工作模型(图2)。在该模型中,SPT-ORMDL复合物作为一个内质网膜上的神经酰胺感受器,可以感知细胞中的神经酰胺水平。在神经酰胺水平比较低的时候,ORMDL的N端高度灵活,使得SPT-ORMDL复合物保持在活性状态,从而增加鞘脂的合成;随着神经酰胺水平的增加,神经酰胺与SPT-ORMDL复合物结合,诱导并稳定ORMDL的N端,形成抑制性构象,阻止底物进入,将复合物转化为非活性状态,使得鞘脂合成减少,以保持细胞中的鞘脂稳态。研究人员也指出,ALS相关的SPT突变体不能正常地感知神经酰胺水平,导致SPT活性不受调节、不受限制的生物鞘脂合成。这些结果表明,在哺乳动物中SPT-ORMDL复合物作为调控鞘脂稳态的神经酰胺感受器,对生物体的健康至关重要。另外,这项研究提出的感知机制,也为生物体内其他生物合成途径的稳态调控提供重要参考。
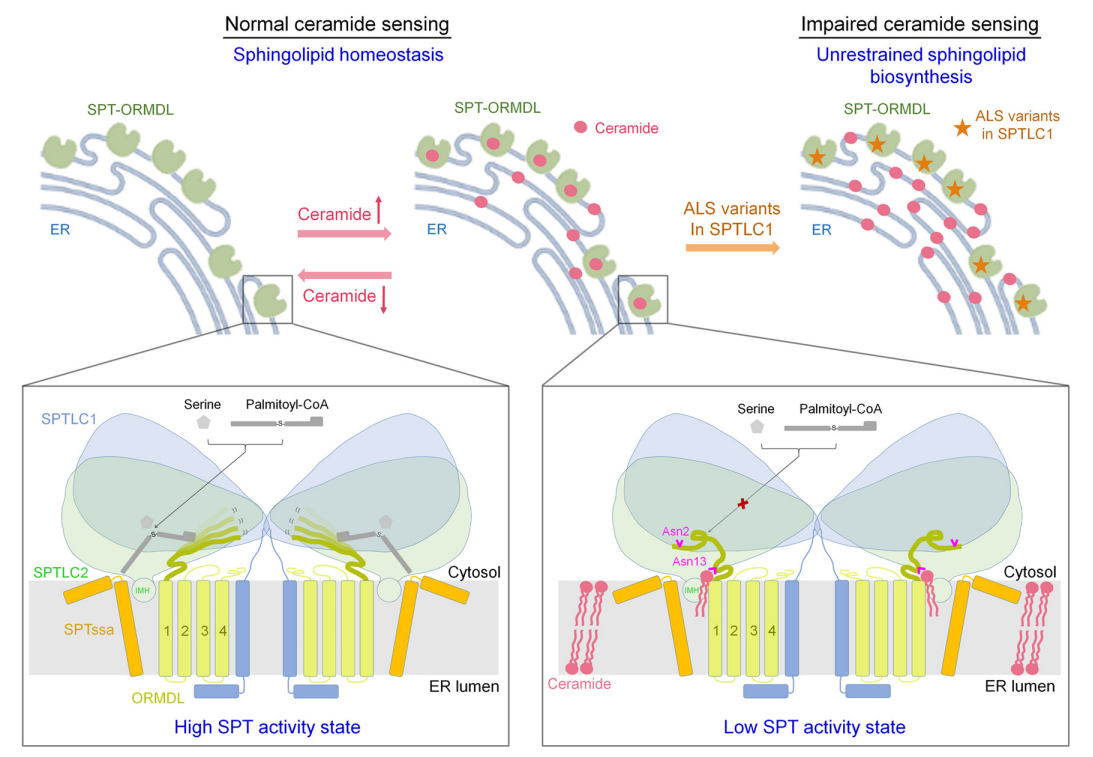
图2. 哺乳动物中鞘脂合成稳态调控的工作模型
南科大生命科学学院研究副教授谢田、博士研究生刘鹏为本论文的共同第一作者,龚欣副教授与美国弗吉尼亚联邦大学Binks W. Wattenberg教授为论文的共同通讯作者。南科大为论文第一单位。该工作得到了国家自然科学基金、广东省科技厅、深圳市科创委的资助。冷冻电镜数据收集和处理得到了南科大冷冻电镜中心的支持,质谱实验得到了分析测试中心的支持。
论文链接:
https://www.nature.com/articles/s41467-023-39274-y
供稿:生命科学学院
通讯员:付文卿
编辑:曾昱雯
最新动态
-
在朋辈交流中走进真实科研,生命科学学院举办“跨系实验室分享会”
Date:2026-05-18
-
生物系青年学者俱乐部成立仪式暨首期“Happy Friday”学术交流活动成功举办
Date:2026-05-18
-
南科大翟继先团队与合作者发布小鼠泛器官Poly(A)尾图谱
Date:2026-05-11
-
南科大董涛教授入选美国微生物学会生命机制前沿探索委员会
Date:2026-05-10
