南科大刘晓天与合作者揭示胶原蛋白半乳糖基化修饰的分子机制
日期:2026-03-27
近日,南方科技大学生命科学学院张明杰院士课题组研究副教授刘晓天与合作者,在国际权威期刊《自然・通讯》(Nature Communications)在线发表题为Molecular basis of collagen galactosylation by GLT25D1的最新研究成果。该研究通过冷冻电镜技术首次解析人源GLT25D1及其三元复合物的高分辨率结构,系统阐明胶原蛋白羟基赖氨酸特异性半乳糖基化的分子机制,揭示致病突变导致功能异常的结构基础,为脑小血管病、骨骼肌肉缺陷等胶原相关疾病的机制研究与精准干预提供重要理论支撑。
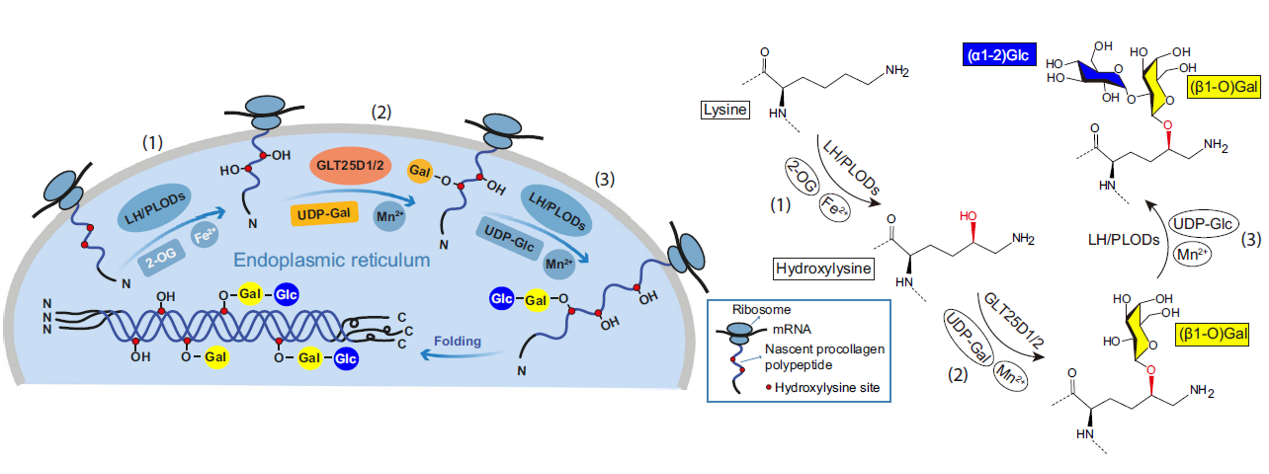
图1. 胶原蛋白修饰通路示意图
胶原蛋白是动物体内含量最丰富的结构蛋白,是细胞外基质核心组分,其翻译后糖基化修饰对胶原成熟、组织稳态维持至关重要。GLT25D1 作为催化胶原糖基化起始步骤的关键半乳糖基转移酶,负责将半乳糖基团转移至胶原特定位点的羟基赖氨酸残基;该酶功能异常与脑小血管病、血管性认知障碍、骨骼肌肉发育缺陷等多种疾病密切相关,但其底物识别、催化反应与寡聚组装的分子机制长期未被解析。
研究团队成功解析人源 GLT25D1 在空载态、UDP 结合态及底物三元复合物态的高分辨率冷冻电镜结构,发现 GLT25D1 单体呈独特双叶结构,可组装成二聚体与六聚体两种功能寡聚形式,其中六聚体以 “三聚二聚体” 方式排列,形成适配胶原三螺旋结构的高效催化平台。结构与生化实验证实,GLT25D1 的N 端结构域(NGT) 高亲和力结合供体底物 UDP‑半乳糖,发挥底物锚定与结构稳定作用;C 端结构域(CGT) 为真正催化中心,通过保守 “Hyl‑Gly” 基序精准识别胶原底物,在 Mn²⁺辅助下完成半乳糖转移反应。团队进一步鉴定出D522为催化关键碱基,明确其通过 SN2 型反转机制完成糖基转移,同时发现底物结合诱导 “盖子环” 构象重排,实现供体与受体底物协同识别与高效催化。研究团队将已报道的 GLT25D1 致病突变精准定位到结构上,发现不同突变通过破坏蛋白折叠、干扰底物结合、削弱催化活性等 distinct 机制导致酶功能丧失,从分子层面解释脑小血管病、骨骼肌肉缺陷等疾病的发病机理,为疾病分型、分子诊断与潜在治疗策略提供关键依据。
综上,该研究完整揭示 GLT25D1 介导胶原半乳糖基化的分子基础,填补糖基转移酶家族与胶原修饰领域关键认知空白,不仅深化对胶原稳态维持机制的理解,也为 GLT25D1 相关罕见病、结缔组织疾病及部分肿瘤的靶向干预奠定重要结构基础。
南方科技大学刘晓天研究副教授、华中科技大学张敏副教授、于洪军教授为论文共同通讯作者。研究得到国家自然科学基金、深圳市医学科学院、南方科技大学冷冻电镜中心等单位资助支持。
论文链接:https://doi.org/10.1038/s41467-026-69234-1
来源:生命科学学院
通讯员:李沐涵
审核:万峻
最新动态
-
在朋辈交流中走进真实科研,生命科学学院举办“跨系实验室分享会”
Date:2026-05-18
-
生物系青年学者俱乐部成立仪式暨首期“Happy Friday”学术交流活动成功举办
Date:2026-05-18
-
南科大翟继先团队与合作者发布小鼠泛器官Poly(A)尾图谱
Date:2026-05-11
-
南科大董涛教授入选美国微生物学会生命机制前沿探索委员会
Date:2026-05-10
